近日,我校孔令义/杨鸣华、赵玉成团队在权威期刊Journal of the American Chemical Society上发表了题为“Biosynthesis of γ-Alkylidenebutenolide Derivatives Reveals an Atom-Deleting Lactone Ring Contraction by Dual-Enzyme Cascade”的最新研究成果。我校博士生李翠萍、博士后付玉状为论文第一作者,孔令义教授、杨鸣华教授和赵玉成教授为通讯作者,中国药科大学为唯一通讯单位。
以α,β-不饱和γ-内酯环为特征的γ-亚烷基丁烯内酯是广泛存在于植物与微生物次生代谢产物中的活性结构单元,但其生物合成途径仍尚未得以解析。研究团队在研究一类具有γ-亚烷基丁烯内酯与环戊烷双环骨架的新颖曲霉代谢产物生物合成过程中,成功揭示了一条具有普适性的δ-取代γ-亚烷基丁烯内酯生物合成途径。该生合过程中,由氧化酶PesD与DUF3237家族酶PesF构成的“双酶级联体系”可通过“原子删除”实现δ-内酯至γ-内酯的缩环过程,是一种化学反应中前所未见的碳骨架编辑机制。
进一步的晶体结构解析与DFT计算表明,PesF的关键残基Glu99先后介导了质子转移和环开裂反应,实现非金属依赖型催化。该机制的阐明不仅丰富了DUF3237酶的新功能,也为生物催化环收缩提供了新模型。该研究为理解天然产物“原子级骨架重构”提供了新范式,并为复杂分子合成和酶工程设计开辟了新的思路。
本研究工作得到了国家自然科学基金面上项目和教育部、外专局高等学校学科创新引智计划(“111”计划)项目的资助。
文章链接:https://doi.org/10.1021/jacs.5c13197
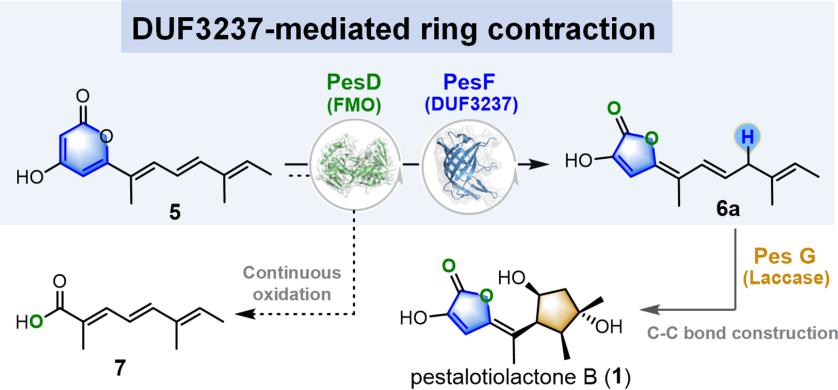
研究的γ-亚烷基丁烯内酯生物合成路径示意图
(供稿单位:中药学院,撰写人:张熙晗,审稿人:刘帆)

