日前,我校黄张建团队与中国科学院生物物理研究所陈畅团队在Redox Biology期刊合作发表了题为“S-nitros(yl)ation of CaMKIIα and its precision redox regulation by SNOTAC plays a critical role in learning and memory”的成果,成功开发出区别于传统一氧化氮(NO)供体的精准亚硝基化调控分子SNOTAC,为改善记忆损伤带来了新的治疗策略。
CaMKIIα亚硝基化修饰:一种介导学习记忆的全新机制
陈畅团队长期致力于研究蛋白质亚硝基化修饰与疾病的关系,其前期工作发现,在老年人和衰老小鼠的海马组织中,负责去亚硝基化的酶GSNOR蛋白表达水平显著升高,而学习记忆关键蛋白钙离子/钙调蛋白依赖性蛋白激酶lla(Ca2+/calmodulin-dependent- protein kinase lla, CaMKllα)的巯基亚硝基化修饰(S-nitros(yl)ation)水平则显著下降(J Neurosci. 2017;37(40):9741-9758.)。这些重要线索提示CaMKIIα亚硝基化修饰下降可能与衰老相关的学习记忆损伤密切相关。
陈畅团队进一步深入探索了这种修饰在学习记忆中的具体作用和因果关系,首次证明CaMKIIα亚硝基化修饰是独立于广泛认知的磷酸化修饰之外,一个全新的介导生理学习记忆功能的关键翻译后修饰。深入的机制研究发现,CaMKIlα一旦失去亚硝基化修饰,会导致神经静息状态下突触前囊泡释放异常(“漏电”效应),证明了其是导致学习记忆下降的新机制,为阐释衰老相关记忆衰退提供了新视角。
精准亚硝基化干预:从概念到实践
明确了CaMKIIα亚硝基化对记忆的核心调控作用,黄张建课题组进一步探索能否通过精准提高其修饰水平来挽回记忆损伤。区别于蛋白乙酰化、磷酸化等翻译后修饰,蛋白亚硝基化修饰尚无普适的合成酶,而主要通过一氧化氮与巯基反应生成。传统调控亚硝基化的方法(调节NO水平)往往“广撒网”,会非特异性地影响众多蛋白质,可能引发脱靶效应。近期,黄张建团队开发了“弹头”策略实现对多种靶标的精准亚硝基化修饰(J Am Chem Soc. 2025, 147(30): 26726−26738)。针对CaMKIIα亚硝基化的精准调控,团队发展了另一种普适的“胶水”策略——即通过小分子将靶蛋白与一氧化氮合酶拉近,使其产生的NO选择性作用于靶蛋白进而实现精准的亚硝基化修饰,创新设计并合成了亚硝基化靶向嵌合体SNOTAC。
本研究开发的精准亚硝基化调控分子SNOTAC能够特异性地将神经型一氧化氮合酶(nNOS)与目标蛋白CaMKIIα拉近,从而精准地、选择性地提升CaMKIIα的亚硝基化水平。通过滴鼻给药方式给予SNOTAC,能够有效挽回因大脑特异性GSNOR过表达(模拟衰老相关的亚硝基化水平下降)而导致学习记忆缺陷的小鼠的记忆能力。此策略具有推广至其他疾病及靶标的潜力,亦可促进药物发现新方法的产生——在深入理解特定蛋白亚硝基化与疾病发生发展的关系基础上,通过对亚硝基化的精准调控从而实现疾病的治疗。这在一定程度上可解决药物研发中有限药物靶标的瓶颈问题,也为创新药物研究提供新思路和新方法。
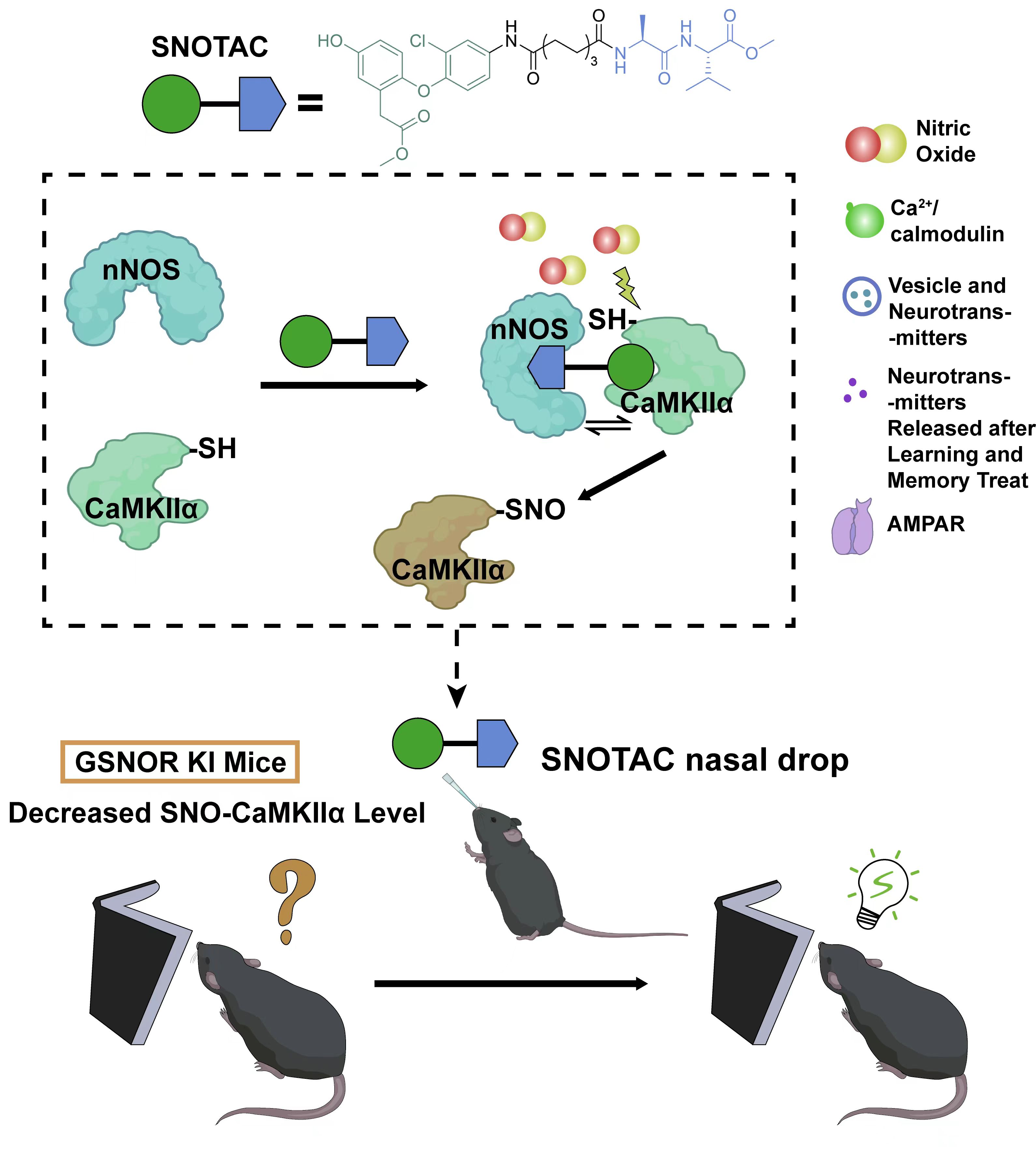
CaMKIIα精准亚硝基化分子SNOTAC改善学习记忆障碍
本研究基于年老忘事关键靶标CaMKIIα的关键亚硝基化位点进行候选药物开发,提出了区别于传统NO供体的全新药物研发策略——“胶水”策略,基于此策略开发的SNOTAC分子实现了精准靶向关键氧化还原修饰以改善学习记忆下降,为精准亚硝基化干预提供了成功范例。
中国科学院生物物理所陈畅研究员和中国药科大学黄张建教授为论文的共同通讯作者。陈畅组褚博煜博士、乔新华副研究员和黄张建组博士后叶辉为共同第一作者。该研究获得了国家重点研发计划、中国科学院战略性先导科技专项(B类)、国家自然科学基金和北京市自然科学基金的资助。
文章链接:https://doi.org/10.1016/j.redox.2025.103784
(供稿单位:多靶标天然药物全国重点实验室,撰稿人:吴建兵,审稿人:刘帆)





