近日,我校生命科学与技术学院刘畅教授团队在权威期刊Advanced Materials发表最新研究成果“Photosensitive Biomimetic Nanomedicine-Mediated Recombination of Adipose Microenvironments for Antiobesity Therapy”。我校已毕业博士研究生宋明明(现就职于安徽医科大学)和2023级硕士研究生王丽为本文的共同第一作者,宋明明博士和刘畅教授为共同通讯作者,中国药科大学为论文第一完成单位。
肥胖症的核心病理在于脂肪组织“代谢-免疫”失衡的恶性循环。现有药物因靶向性差、控释能力不足及脱靶毒性,难以实现代谢重编程与免疫微环境调控的协同增效。为解决这个问题,刘畅教授课题组提出一种“代谢—免疫双向协同调控”新策略,通过靶向抑制巨噬细胞M1极化并激活PPARγ介导的白色脂肪组织褐变,实现炎症消退与代谢改善的协同增效。
为此,刘畅教授课题组设计了一种新型的红光响应型仿生纳米递药系统—RSCP NPs。该系统通过脂肪靶向肽修饰生物膜仿生载体,精准靶向白色脂肪组织炎症区域,并利用红光/pH双响应系统实现药物精准时空控释。研究结果表明,RSCP NPs能将虾青素和罗格列酮递送至M1型巨噬细胞和白色脂肪细胞,缓解白色脂肪组织低度炎症并促进棕色化,并通过组学分析揭示了“代谢—免疫双向协同调控”的关键节点。该研究为新型药物递送系统在代谢性疾病中的开发和应用提供了理论依据和实践基础。
以上研究工作获得国家自然科学基金面上项目、国家重点研发计划项目、江苏省自然科学基金、安徽省自然基金、新疆维吾尔自治区自然科学基金以及中国药科大学多靶标天然药物全国重点实验室研究项目的资助。
全文链接:https://doi.org/10.1002/adma.202417377
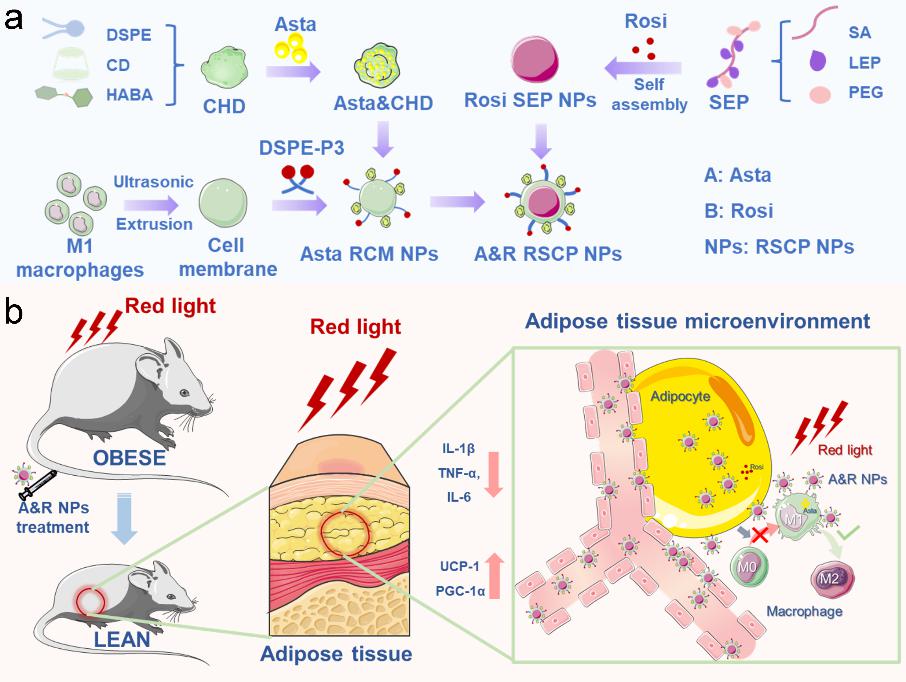
示意图
(供稿单位:生科院,撰写人:夏露,审稿人:刘帆)





