化疗耐药与系统毒性长期制约肿瘤治疗效果的提升。尽管ROS响应型前药被视为拓展化疗治疗窗的重要策略,但传统连接子多遵循“氧化剂消耗型”机制,即依赖化学计量消耗ROS实现药物释放。在内源性ROS水平受限且抗氧化体系活跃的肿瘤微环境中,这类策略往往面临触发效率不足与释放受限的双重瓶颈。针对上述关键科学问题,郑月钦教授团队创新性地提出“ROS催化放大”新范式,设计并构建了一类基于苯硒基环己烯酮骨架的催化性ROS放大型自消除连接子。该策略首次将ROS响应性断裂与有机硒介导的氧化还原循环耦合于单一小分子体系,使ROS由“单次触发信号”转变为“可持续放大的治疗驱动力”。这一设计不仅显著提升了前药激活效率,还在低ROS环境中实现自增强释放,为难治性肿瘤提供了一种无需载体的全新小分子前药设计思路,具有明确的机制创新与化学工具属性。
相关成果以“Catalytic ROS-Amplifying Self-Immolative Linkers Enable Carrier-Free Prodrugs for Refractory Tumors”为题发表于Angewandte Chemie International Edition。论文由我校博士研究生周祺为、本科生韩煜霖以及江苏省人民医院(南京医科大学第一附属医院)胰腺中心王亚洲共同担任第一作者,中国药科大学为第一通讯单位。
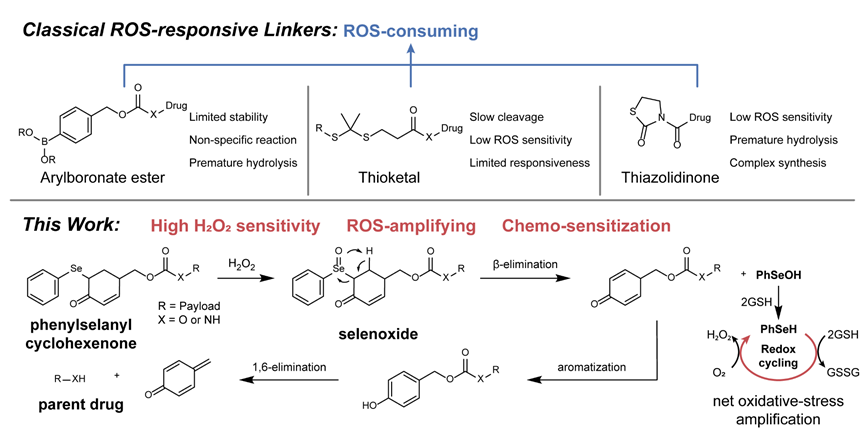
图1.催化性ROS放大型自消除连接子的设计
在疼痛管理领域,开发安全且高效的非阿片类镇痛策略仍是尚未解决的难题。局部麻醉药虽然具有替代阿片类药物的潜力,但传统药物缺乏神经选择性,往往同时阻滞感觉与运动神经,导致运动功能受损。2′,6′-Pipecoloxylidide已被证明是一种具有感觉选择性的局部麻醉药,但其选择性高度依赖局部浓度,亟需可精准调控的递送与释放策略。围绕这一核心难题,团队提出“光控时空精准释放”策略,创新性构建了一种红光触发的click-release前药体系。该体系首次在体内实现了可重复、可编程的感觉选择性阻滞,同时几乎不影响运动功能。这一创新不仅验证了光控前药用于精准镇痛的可行性,更为临床上实现"按需镇痛"的个体化疼痛管理开辟了全新路径。
论文以Precise Spatiotemporal Control of Sensory Nerve Blockade via Light-Triggered Click-Release Uncaging of 2′,6′-Pipecoloxylidide为题在Angewandte Chemie International Edition上发表。由我校博士研究生陈双龙、硕士研究生王义臣以及博士研究生程铭鑫共同担任第一作者,中国药科大学为第一通讯单位。
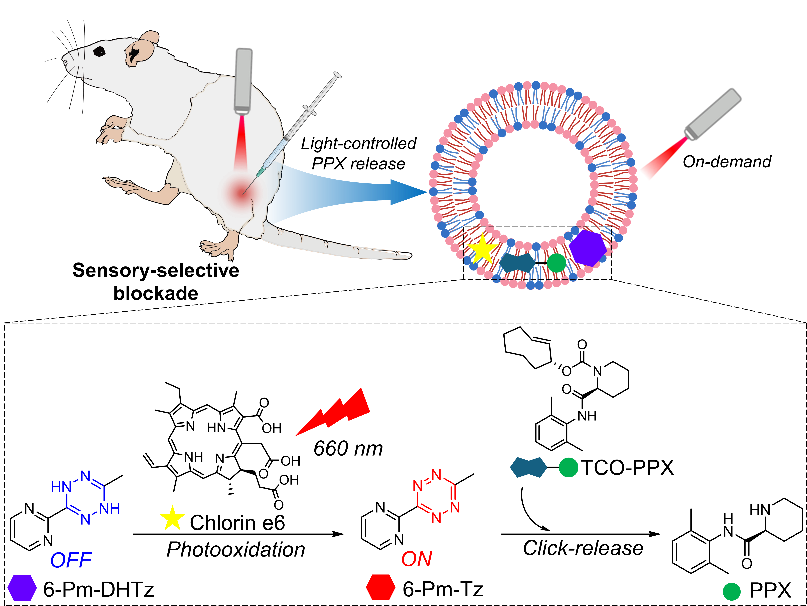
图2.红光触发的感觉选择性阻滞
(供稿单位:多靶标天然药物全国重点实验室,撰稿人:陈家轩,审稿人:刘帆)





